�Ӿ���ҽ��ת��Ϊѭ֤ҽѧ�Ĺ��̣�����ҽ��ͬ���Ƕ��ھ����Ĺ��̡�
�������Ⱦ�������У�ѭ֤ҽѧ�����۲������������κ�ҽ�ƾ��߶�Ӧ��������ѿ�ѧ�о�֤�ݻ����ϣ������������Ǹ�����ʶ����Ч���ƿ��������ã����ⳬ��ϸ���IJ�����

������������ļ��������۵��ռ���������ҽ��ʼ��ʶ�������Ⱦʱ��������������ҩ���������Ҫ�ԡ�ҩ������Ŀ����ɸѡ���п������Դﵽ��Ч�Ŀ������ƣ��Ӷ������������ڣ����ٶ���ʹ�ࡣ
�ٴ�ҽʦӦ����ҩ��������������ѡ������Ч��ҩ��������ƣ������յ����õ���Ч��ҩ������Ҳ��Ժ�ڸ�Ⱦ�����в�ѧ����������ֶ�֮һ���ɼ�����ҩ���������ҩ����̬�仯��������ҽԺ�ƶ����η�����������ҩ������������ҩ�������ǿԭ����ҩ������ҩ�ԣ������ƴ������ѡ�
Ŀǰ�����ٴ������У�������ѡ��ҩ�ﻹ�DZȽϳ����ģ�һ�����������ҩ���ٿ���ҩ��ʵ���п����Ѿ��������Ƶ����ʱ�ڡ�
Ŀǰ������ʵ���ҿɽ���ϸ������������������ҩ�����飬��ĸ�����������������ҩ�����飬Ƥ����ԭ�������������ೣ���������ֶΡ�
������Ҫ����ϸ��������ҩ���ı��������ٴ�����������ɡ�����Ч��������ҩ����һ�µ�ԭ�� ��
ϸ��������������������������������Ը��ֳ�����ԭ����һ�ּ�ⷽ����ʹ����������ķ����������²��IJ�ԭ����ͨ�����߷���������ͼ1�����������������ɾ��䴿����������ѡ����������ѡ���ԣ�ͼ2�����Դ˷������������ɲ�ԭ����
��һ��ͨ��������Ⱦɫ��ϸ����Ϊ���ࣺ�������Ծ����������Ծ���ͨ��������̬�۲죬ȷ���Ƿ�Ϊ�������������������Ը˾���ͼ3����
��һ������ͨ�������Ĵ�ø���飬���������������Ϊ��������������������ͨ������ø��O/F�������齫�������Ը˾���Ϊ���˾����ͷǷ��;����������ϸ��������ҩ���������н������յ�����������ͼ4 ����
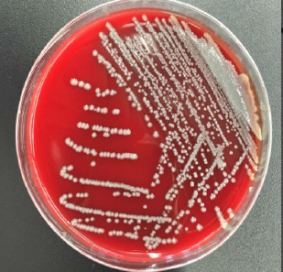
ͼ 1 ���˾�����Ѫ��֬����̬
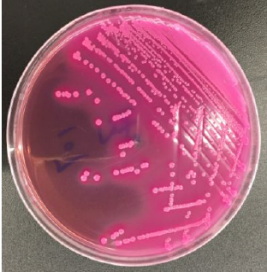
ͼ 2 ��ϣ����MAC����̬
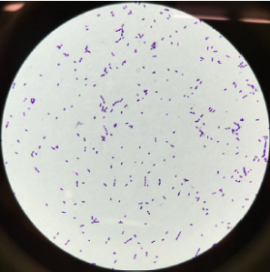
ͼ 3 �������������
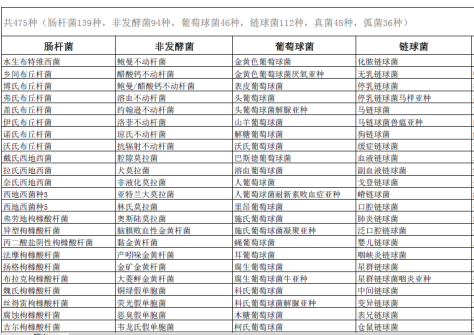
ͼ 4 �ɱ�������ֽ�ѡ
ϸ���������ȷ�����������Ըþ��ֵ�ҩ��ѡ���Լ�ҩ�����顣ʵ���Ҳ�������ʵ���ұ�ίԱ�ᣨNCCLs�������±�����ҩ�����顣���ݲ�ͬ��ԭ������ԭ�����ڲ�λ��ҩ;�����Լ�ҩ������ѧѡ���д����Ե�ҩ����ҩ�����顣��ҩ�������Ϊ��ѡҩ����ѡҩ����·��Ⱦҩ�
��ѡҩ����Բ�ͬ��ԭ�������ѡ��ѡҩ�ǻ������ѡҩ�����л�Ը�ҩ���������ʹ�õ������ѡ�ã���·��Ⱦֻ������·��Ⱦʱѡ�á�
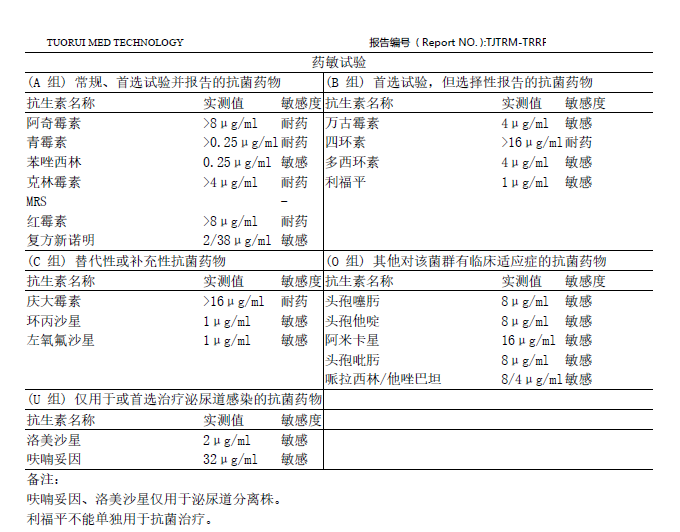
ͼ5 һ��MRS���Ե����������ҩ�����鱨��
��������
���� �������汨�桢��ѡ�����ҩ����ϣ��Լ�һЩ���ض���Ⱥ�ij������鱨�档
���� ����һЩ����������ѡ�����ҩ����ǣ�����ֻ�DZ�ѡ���Եر��棬���統ϸ���ԣ���ͬ��ҩ����ҩʱ������ѡ�á�
C�� ��������Ի��Կ�����ҩ�������������������飺ijЩ��λ������DZ���ж�һ�ֻ����ֻ���ҩ��(�ر��Ƕ�ͬ��ģ���β-��������)��ҩ�ģ��ֲ����л�㷺���еľ��ꣻ���ƶ���ѡҩ������Ļ��ߣ������ټ����ĸ�Ⱦ(����ù�ضԳ������Ⱦɳ�ž����������ijЩ�����ù����ҩ�ij����)�������������в�ѧ�ĸ�Ⱦ���Ʊ��档
U�� (“�����”) �г���ijЩ�����������������Ⱦ�Ŀ�����ҩ(��������ijЩ�ŵͪ��ҩ��)����������⣬������Ⱦ��λ����IJ�ԭ�����ô���ҩ��������顣�����и��㷺��Ӧ֢��ҩ���������U ������������������������ԭ�����磬ͭ�̼ٵ���������
O�� ( “����” ) �Ը���ϸ�����ٴ���Ӧ֢����������һ�㲻���������뱨��ĺ�ѡ��
Inv ��( “�о���” ) �Ըþ�Ⱥ���о�������δ��FDA����ҩ�
���ڽ��ͨ��ʹ�����У�S�����н飨I������ҩ��R�������֡������е����С��н����ҩ���䶨�����£�
����(S)“����”�� ��ʾ���Ը�Ⱦ��λʹ���Ƽ�����ʱ���þ���ͨ����������ҩ��Ũ�ȿɴﵽ��ˮƽ�����ơ�
�н�(I)“�н�”�� ������Щ���꣬�俹����ҩ��MIC �ӽ���ѪҺ����֯��ͨ���ɴﵽ��ˮƽ����������ҩ���Ƶķ�Ӧ�ʿ��ܵ��������ꡣ“�н�”������ζ��ҩ��������Ũ����λ�����ٴ�Ч��(����Һ�е��ŵͪ���β����������)���߿��ø�������������ҩ���������(��β����������)���˷������һ���������������Ա���С�ġ�δ�ܿ��Ƶļ�����������ش�Ľ�����ʹ����ر��Ƕ���Щҩ�ﶾ�Է�Χխ��ҩ�
��ҩ(R) “��ҩ”�� ��ָ��������������ڿ�����ҩͨ���ɴﵽ��Ũ��ʱ�����겻�ܱ����ƣ���/�ͱ����־�Ȧֱ����С��������ܲ����������������ҩ���ƣ���β-������ø���ķ�Χ�ڣ����������о���ʾҩ��Ծ����ٴ���Ч�����ɿ���
����Ҫ�Ա�����н��ʱ����Ҫע�����¼��㣺
?. ϸ���Զ������ǵ�ҩ������ǹ̶��ġ�������������Ҫ���о��ּ�������Ϊÿ�־�����Ӧ��ҩ��ѡ���Dz�ͬ�ģ�
?. ijЩϸ����ij��ҩ�������Ȼ��ҩ������Ҫ��ҩ���������顣���糦�����ͷ����Ȼ��ҩ���ٴ�ӡ֤���ڲ�ͬ���Ŀ�����ѡ�����Ҫ�����äĿ��ȥ��ҩ���������飬��ʱ������ܲ����ܷ�ӳ�����������
?. �����ҩ���������һ��ҩ�������ֻ��������ҩ������� ͼ6 �У���ù���뱽�����ֿ���Ԥ���β-��������ҩ�������Ƿ���ڶ�����ҩ��
?. ��Ϊ������ҩ�����飬��Щҩ���������У������ٴ�������Ч
?. ͬһ������ܳ������֣���������ҩ�����鲻ͬ�������Է���ͬ�걾��ҩ���������ʵ���Ҽ�ԱȲ������壩
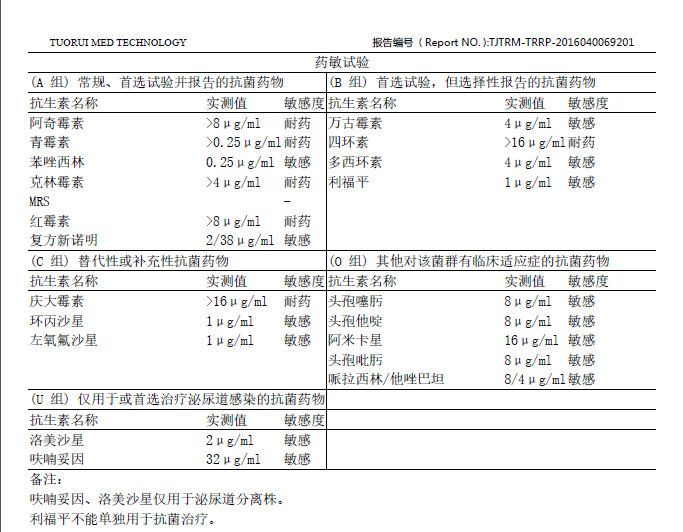
��һ��ʵ�������ٴ���ͨʱ����������
���� 7���ٴ��������� ���
Q1��Ϊʲô�������õ�ҩ����ҩ��������û������
A1��1������Ϊ��Ȼ��ҩ��2��������ҩ�������Ա�����ҩ����Ԥ����
Q2��Ϊʲô�е�ϸ������ܶ���ҩ��еĽ����漸�֣�
A2�������ҩ��������ϸ�������������ͭ�̼ٵ����������ҩ������࣬������ѿխʳ�����������ҩ�������١����ٴ�ǿ�����ּ�������Ҫ�ԣ�
Q3���Ƿ��ܽ�ʹ�õ�ҩ����ҩ�����飿
A3��û�б�ҪҲ��̫���ܡ�
1��ͨ����ҩ���ƺͱ�־��ҩ�����Ԥ����������ҩ�������ԣ�
2������������ҩ��������ҩ�����飬��Ҫҩ���������ȶ��������в������ͽ��ͱ��ſɡ�
Q4���������Ե�ϸ������Ҫ���п�����������
A4����������≠��Ⱦ������Ϊ��Ⱦ����ֲ�����κν����Ҫ����ٴ�����������ۡ���Ⱦ��λ���崴����������ҩ��ʱҪ��ҩ�����Ƹ�����Ҫ……
Q5��Ϊʲôҩ���������е�ҩ����ٴ���������Ч��
A5������ҩ������ֻ��Ԥ����������Ч������������Ϊ��ҩ��������Ч��
����≠������Ч��
��ԭ�����Ϊ: 1�����ܲ����������²���������Ⱦ����ֲ������2��ϸ�����������յ���ҩ���ƻ����ﱻĤ��3����Ⱦ��λ��ҩ������ѧ���أ�4��ϸ����MIC����ҩ�ļ�����ҩ��ʽ���أ�5��ҩ����������Щҩ�ﵥ��ʹ����Ч����Ҫ����������������ҩ; 6��ҩ����ͼ��������ö����ء�
Q6��ͿƬ������������������Ǻϣ�
A6��1��ͿƬ����Ϊ���пɼ����ϸ������������Ŀ�����ڼ���²�����2��һЩ����������������²ſ�������
Q7��ȡ�����Ծ���ŧҺ�걾������Ϊ�������ԣ�
A7��1��ʵ����Ŀǰ��չ��Ϊ�����������������������������Ϊ��������Ⱦ���������ԣ�2������ϸ��������������ϸ�����ɡ�
ȷ�ж���淶����

���ڻ��崦�ڸ��ӵ���̬����������������������ҩ������Ľ��������ٴ������ش�
���ٴ������У���淶�ͼ졢���͡�������������ҩ�����̡�ÿ��ϸ�ڶ���Խ����ɾ�Ӱ�졣����ϵ�����ظ�Ⱦʱ���ٴ���ͬʱ�ͼ�����Ѫ�����͵���Ѫ����Ҫʱ�ͼ쵼�ܼ⡣���ٴ���Ѫ�������ͼ�����Ƶ�ʡ�ʱ����������ر������
�������ҶԽ���ж�������ȱ����Ч�Ļ��ơ�������ȷ�ĵ��ܼ������������Ӧ���ǣ��������>15 CFU����ʾCRS��������G+b�����м�����ҩ�����������<15 CFU��������һ����Ҫ�ľ�������AȺ��G-b���������̫����>100 CFU������������ϻ�G-bʱ����δ��Ѫ������Ӧ����“����Ѫ����������Ƿ���������ظ�Ⱦ”���붨��ƽ��96h�����棨Ҫ����Ѫ��������
������Ч��������ҩ����һ�µ�ԭ��
1. ����ҩ���Ӧ�û����Խ��������������ʡ�ǿ����ʹ�ÿ�����ǰ��ȡ�걾��
2. �걾����ȷ�ɼ������䳣����������ϼ����ɹ��Ĺؼ����ڡ���̵����Ϊ����ͨ��ͿƬ���췢�ֲ��ϸ��߲����������ϸ�걾������3+��4+�ľ����п������²�����Ѫ���������IJ�Ѫ��ʽ��ÿ�����̲�λ�ֱ������������������ƿ�ӣ�����2�����̵㣬��սǰ1h��Ѫ�������ʽϸߡ������IJ�ԭ������߾���ū���������Ƥ������֯��Ⱦ����֯�걾���������������Ը��ڵ���ŧҺ���������걾�輰ʱ�ʹ�ʵ���Ҳ���ʱ�������������ɼ����Ի�����ԵĽ����
3. ��Ȼ����Һ��Ѫ���Լ�Һ�Ϻ������걾�����ţ�������λ������Ҳ���ܻ���Ⱦ������ø������������ѳ�ΪѪ������Һ����������IJ�ԭ������������ʾ����Ⱦ�ʸߴ�80%���ϡ�
4. �������걾���ж���Ⱦ���Ⱦʱ�������ѡ��ܶ����������ֻ�Ƕ�ֲ�����Ǹ�Ⱦ����Ҫ����ٴ��жϡ�
5. ����ѧ���������ϸ�˽��ͼ�걾����������������ԭ���ʱ�䡢��ͬ��λ����������ȣ�ͬʱ����ٴ������ۺ��жϡ�
6. ҩ���ж��۵���Ҫ��ʱ���£��ر�Ҫ��������CLSI�ļ���



